Диагностические среды. Дифференциально – диагностические среды: перечислить основные виды, принципиальный состав, назначение и использование в практике. Бактериальный нуклеоид содержит
Дифференциально-диагностические среды - специальные смеси питательных веществ, применяемые для определения видовой принадлежности микробов и изучения их свойств. При росте бактерий на дифференциально-диагностических средах протекают химические процессы, обусловленные наличием у микробной клетки различных ферментов. Одни из них способны расщеплять белки , другие - углеводы , третьи - вызывать реакции окисления и восстановления и т. д. Благодаря действию ферментов в дифференциально-диагностической среде происходят соответствующие изменения.
Дифференциально-диагностические среды можно разделить на четыре основные группы.
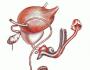
Рис. 1-6. Различные формы расщепления желатины. Рис. 7 - 9. Жидкая среда с углеводом и индикатором Андраде: рис. 7 - отсутствие ферментации; рис. 8 - ферментация с образованием кислоты ; рис. 9 - ферментация с образованием кислоты и газа. Рис. 10 - 12. Полужидкая среда с углеводом и индикатором BP (из сухой питательной среды): рис. 10 - отсутствие ферментации; рис. 11 - ферментация с образованием кислоты; рис. 12 - ферментация с образованием кислоты и газа. Рис. 13-15. Искусственная лакмусовая сыворотка по Зейтцу: рис. 13 - отсутствие ферментации; рис. 14 - ферментация с образованием кислоты; рис. 15 - ферментация с образованием щелочи . Рис. 16 и 17. Молоко с метиленовым синим: рис. 16 - отсутствие редукции; рис. 17 -редукция. Рис. 18 и 19. Среда Симонса: рис. 18 -отсутствие ассимиляции цитрата; рис. 19 - ассимиляция цитрата. Рис. 20 - 24. Лакмусовое молоко: рис. 20 - отсутствие ферментации; рис. 21 - ферментация с образованием кислоты; рис. 22 - ферментация с образованием щелочи; рис. 23 - пептонизация; рис. 24 - редукция. Рис. 25. Разжижение свернутой сыворотки (в проходящем свете). Рис. 26. Гемолиз на кровяном агаре (в проходящем свете). Рис. 27. Кровяная среда с теллуритом калия.
1. Среды, содержащие белок и выявляющие способность микробов расщеплять белки (протеолитические Свойства): мясо-пептонная желатина «столбиком», свернутая лошадиная или бычья сыворотка, молоко, кровяной агар. При посеве бактерий проколом в мясо-пептонную желатину, «столбиком» в случае расщепления белка наблюдают разжижение среды. При посеве на среду со свернутой сывороткой расщепление белка определяют по разжижению среды и образованию углублений на ее поверхности. Расщепление микробом молока выявляется просветлением или растворением первоначально свернувшегося молока. Наличие гемолитической активности исследуемой культуры проверяют посевом ее в чашку Петри на специальный кровяной агар. В результате разрушения эритроцитов вокруг колоний (например, гемолитического стрептококка или стафилококка) образуются зоны просветления.
2. Среды для выявления способности микробов расщеплять углеводы и высокоатомные спирты (Эндо среда, Левина среда, Расселла среда, Дригальского - Конради среда, Рапопорт - Вайнтрауба среда, Шустовой среда). Для выявления этих свойств микроорганизмов применяют также «пестрый» ряд, т. е. серию пробирок, содержащих питательные среды, включающие различные углеводы, многоатомные спирты и индикатор. В качестве индикаторов пользуются лакмусовой настойкой или бромтимоловым синим. Разложение какого-либо из углеводов с образованием кислоты выявляют по изменению цвета индикатора, образование газа- по заполнению газом и всплыванию специального стеклянного поплавка в жидкой среде. Или применяют полужидкие Гисса среды (см.) с 0,5% агара с соответствующими сахарами и индикатором Андраде. После посева микроба на эти среды образование кислоты выявляют покраснением среды, а образование газа - по появлению его пузырьков в агаре или по разрыву и сдвигу вверх агарового столбика. К дифференциально-диагностическим средам второй группы относят также крахмальный агар, служащий для определения способности микробов расщеплять крахмал , среду Кларка и др.
3. Среды, на которых выявляется способность микробов обесцвечивать красители , добавленные к бульону: метиленовый синий, тионин, лакмус, индигокармин , нейтральный красный или другие (среда Ротбергера, среда Омелянского). К третьей группе относят также среды с нитратами, служащие для определения способности микробов восстанавливать соли азотной кислоты (нитраты) в соли азотистой кислоты (нитриты) и далее в аммиак или свободный азот.
4. Среды, выявляющие способность микробов усваивать вещества, которые не усваиваются другими микробами, например среда с лимоннокислым натрием (цитратный агар Симонса) для отличия кишечной палочки, которая лишена способности ассимилировать эту среду, от других бактерий кишечной группы или среда с олеиновокислым натрием для дифференциации дифтерийной палочки от ложно дифтерийной и дифтероидов (агар Энжеринга).
К дифференциально-диагностическим средам относят также среды для дифференциации анаэробов, теллуритовые среды для дифференциации дифтерийных бактерий, среды с мочевиной, щелочные среды (Дьедонне агар) для культивирования холерного вибриона и др. См. также Идентификация микробов.
Дифференциально-диагностические среды - это специальные смеси питательных веществ, применяемые для определения видовой принадлежности микробов и изучения их свойств. При росте бактерий на дифференциально-диагностических средах протекают химические процессы, обусловленные наличием у микробной клетки различных . Одни из них способны расщеплять , другие - , третьи - вызывать реакции окисления и восстановления и т. д. Благодаря действию ферментов в дифференциально-диагностической среде происходят соответствующие изменения.
Дифференциально-диагностические среды можно разделить на четыре основные группы.
Рис. 1-6. Различные формы расщепления желатины. Рис. 7 - 9. Жидкая среда с углеводом и индикатором Андраде: рис. 7 - отсутствие ферментации; рис. 8 - ферментация с образованием кислоты; рис. 9 - ферментация с образованием кислоты и газа. Рис. 10 - 12. Полужидкая среда с углеводом и индикатором BP (из сухой питательной среды): рис. 10 - отсутствие ферментации; рис. 11 - ферментация с образованием кислоты; рис. 12 - ферментация с образованием кислоты и газа. Рис. 13-15. Искусственная лакмусовая сыворотка по Зейтцу: рис. 13 - отсутствие ферментации; рис. 14 - ферментация с образованием кислоты; рис. 15 - ферментация с образованием . Рис. 16 и 17. Молоко с метиленовым синим: рис. 16 - отсутствие редукции; рис. 17 -редукция. Рис. 18 и 19. Среда Симонса: рис. 18 -отсутствие ассимиляции цитрата; рис. 19 - ассимиляция цитрата. Рис. 20 - 24. Лакмусовое молоко: рис. 20 - отсутствие ферментации; рис. 21 - ферментация с образованием кислоты; рис. 22 - ферментация с образованием щелочи; рис. 23 - пептонизация; рис. 24 - редукция. Рис. 25. Разжижение свернутой (в проходящем свете). Рис. 26. Гемолиз на кровяном агаре (в проходящем свете). Рис. 27. Кровяная среда с теллуритом калия.
1. Среды, содержащие белок и выявляющие способность микробов расщеплять белки (протеолитические Свойства): мясо-пептонная «столбиком», свернутая лошадиная или бычья сыворотка, молоко, кровяной агар. При посеве бактерий проколом в мясо-пептонную желатину, «столбиком» в случае расщепления белка наблюдают разжижение среды. При посеве на среду со свернутой сывороткой расщепление белка определяют по разжижению среды и образованию углублений на ее поверхности. Расщепление микробом молока выявляется просветлением или растворением первоначально свернувшегося молока. Наличие гемолитической активности исследуемой культуры проверяют посевом ее в на специальный кровяной агар. В результате разрушения вокруг колоний (например, гемолитического или ) образуются зоны просветления.
2. Среды для выявления способности микробов расщеплять углеводы и высокоатомные (Эндо среда, Левина среда, Расселла среда, Дригальского - Конради среда, Рапопорт - Вайнтрауба среда, Шустовой среда). Для выявления этих свойств микроорганизмов применяют также «пестрый» ряд, т. е. серию пробирок, содержащих , включающие различные углеводы, многоатомные спирты и индикатор. В качестве индикаторов пользуются лакмусовой настойкой или бромтимоловым синим. Разложение какого-либо из углеводов с образованием кислоты выявляют по изменению цвета индикатора, образование газа- по заполнению газом и всплыванию специального стеклянного поплавка в жидкой среде. Или применяют полужидкие Гисса среды (см.) с 0,5% агара с соответствующими сахарами и индикатором Андраде. После посева микроба на эти среды образование кислоты выявляют покраснением среды, а образование газа - по появлению его пузырьков в агаре или по разрыву и сдвигу вверх агарового столбика. К дифференциально-диагностическим средам второй группы относят также крахмальный агар, служащий для определения способности микробов расщеплять крахмал, среду Кларка и др.
3. Среды, на которых выявляется способность микробов обесцвечивать красители, добавленные к бульону: метиленовый синий, тионин, лакмус, нейтральный красный или другие (среда Ротбергера, среда Омелянского). К третьей группе относят также среды с нитратами, служащие для определения способности микробов восстанавливать соли азотной кислоты (нитраты) в соли азотистой кислоты (нитриты) и далее в аммиак или свободный азот.
4. Среды, выявляющие способность микробов усваивать вещества, которые не усваиваются другими микробами, например среда с лимоннокислым натрием (цитратный агар Симонса) для отличия кишечной палочки, которая лишена способности ассимилировать эту среду, от других бактерий кишечной группы или среда с олеиновокислым натрием для дифференциации дифтерийной палочки от ложно дифтерийной и дифтероидов (агар Энжеринга).
К дифференциально-диагностическим средам относят также среды для дифференциации анаэробов, теллуритовые среды для дифференциации дифтерийных бактерий, среды с мочевиной, щелочные среды (Дьедонне агар) для культивирования холерного вибриона и др. См. также Идентификация микробов.
Среда Штерна. Используют для дифференциации сальмонелл. К 1000 см 3 МПБ или бульона Хоттингера добавляют 2,5 см 3 10%-ного насыщенного спиртового раствора основного фуксина, 16,6 см 3 10%-ного водного раствора натрия сульфита (Na 2 S0 4) и 10 см 3 глицерина. Разливают по пробиркам и стерилизуют 15 мин при 112° С. Готовая среда имеет желтую окраску. Если испытуемая культура относится к S. typhimurium, которая способна ферментировать глицерин, то среда приобретает фиолетовый оттенок.
Среда Биттера. Используют для дифференциации сальмонелл. В 1000 см 3 дистиллированной воды растворяют 0,05 г пептона, 0,5 г натрия цитрата, 5 г натрия хлорида, 5 г рамнозы (или арабинозы). Кипятят на водяной бане 3-5 мин, фильтруют через бумажный фильтр. Разливают по пробиркам и стерилизуют 30 мин при 112° С или текучим паром 3 дня подряд по 30 мин. Если испытуемая культура относится к сальмонеллам, способным ферментировать рамнозу или арабинозу (S. typhimurium), то при добавлении к суточной культуре (выращенной на данной среде) 2 капель 0,5%-ного спиртового раствора метилового красного среда приобретает красную окраску.
Среда для посева по Свену -Гарду. Используют для выявления у сальмонелл специфической фазы жгутикового антигена. К 1000 см 3 МПБ или бульона Хоттингера добавляют 8 г агара и растворяют путем кипячения на водяной бане. Устанавливают рН 7,2-7,4, фильтруют через бумажный фильтр и стерилизуют 30 мин при 121° С.
Среды с аминокислотами. Используют для определения способности энтеробактерий в анаэробных условиях расщеплять левовращающие аминокислоты - лизин, орнитин, аргинин. В 600 см 3 дистиллированной воды растворяют 5 г пептона и 1 г глюкозы, устанавливают рН 6,0-6,1. Приготовленный раствор разливают по 150 см 3 в четыре колбы. В каждую из трех колб вносят по 10 г одной из аминокислот. Четвертая колба остается в качестве контрольной. Содержимое всех колб кипятят на водяной бане 5-10 мин, устанавливают рН 6,0-6,1. Во все че тыре колбы вносят по 0,6 см 3 1,6%-ного спиртового раствора бромкрезоло-вого пурпурного или бромтимолового синего и по 5 см 3 0,1%-ного спиртового раствора крезолового красного. Разливают в агглютинационные пробирки по 2-3 см 3 и стерилизуют 30 мин при 110° С.
Для проведения теста в пробирки, содержащие аминокислоту, и в контрольную пробирку засевают испытуемую культуру, после чего заливают стерильным вазелиновым маслом (слоем толщиной 10 мм) и инкубируют. Учет проводят в течение 4 сут. При положительной реакции среды с аминокислотами приобретают фиолетовую или синюю (в зависимости от индикатора) окраску, в контрольных пробирках среда имеет желтую окраску.
Состав 1,6%-ного спиртового раствора бромкрезолового пурпурного: бромкрезоловый пурпурный - 1,6 г, спирт этиловый 96° - 100 см 3 .
Состав 0,1%-ного спиртового раствора крезолового красного: крезоловый красный - 0,1 г, спирт этиловый 96° - 100 см 3 .
Среды, содержащие органические кислоты. Используют для дифференциации сальмонелл по их способности расщеплять органические кислоты (тартраты, мукаты, натрия цитрат). В 1000 см 3 дистиллированной воды растворяют 10 г пептона, добавляют 8,5 см 3 0,1 Н раствора натрия гидроокиси, 12 см 3 0,25%-ного водного раствора бромтимолового синего, 10 г D-тартрата (или одну из следующих кислот: 5 г L-тартрата, 5 г мезотартрата, 10 г муката, 10 г натрия цитрата). Устанавливают рН 7,4, разливают в пробирки и стерилизуют 20 мин при 112° С. Готовая среда синезеленого цвета. При положительной реакции в процессе инкубации среда с культурой приобретает зелено-желтую окраску.
Для получения более четких результатов в конце срока инкубации в пробирки с сомнительной или отрицательной реакцией добавляют несколько капель насыщенного раствора ацетата свинца, в результате при отрицательной реакции выпадает обильный осадок (до 2 / 3 объема среды), при положительной - выпавший осадок незначителен.
Среда с триптофаном.
Используют для определения у бактерий наличия триптофандезаминазы. В 1000 см 3 дистиллированной воды растворяют 2 г DL-триптофана. Устанавливают рН 6,7-6,9. Для определения способности бактерий к дезаминированию триптофана испытуемую агаровую культуру бактериологической петлей вносят в пробирку с 0,5 см 3 раствора триптофана и инкубируют 30 мин при 37° С, после чего вносят
1 каплю 10%-ного водного раствора железа хлористого трехвалентного (FeCl 3). При положительной реакции среда приобретает темно-красную окраску, при отрицательной - желтую.
Среда с калием цианидом. В 1000 см 3 дистиллированной воды растворяют 10 г пептона, 5 г натрия хлорида, 0,225 г калия дигидрофосфата (КН 2 Р0 4), 5,64 г натрия гидрофосфата (Na,HP0 4). Устанавливают рН 7,6, фильтруют через бумажный фильтр и стерилизуют 30 мин при 112° С. После стерилизации быстро охлаждают. Среду этого состава используют в качестве контрольной. Непосредственно перед применением к 100 см 3 среды асептически добавляют 1,5 см 3 свежеприготовленного 0,5%-ного водного раствора калия цианида (KCN), разливают по пробиркам и закрывают корковыми пробками.
Пробу считают положительной, если через 24-48 ч после посева культуры в среде заметно помутнение или опалесценция. При отрицательном результате среда остается абсолютно прозрачной, в то время как в контрольной пробирке заметно помутнение.
Среда Клиглер. Используют для определения образования сероводорода. В 1000 см 3 МПБ растворяют при кипячении 20 г пептона, 5 г натрия хлорида, 0,4 г натрия сульфида, 0,08 г натрия тиосульфата, 20 г агара. Устанавливают рН 7,8, затем снова кипятят, фильтруют через бумажный фильтр и добавляют 0,5 г железа сернокислого, растворенного в небольшом количестве воды, 10 г лактозы, 1 г глюкозы и 12 см 3 0,2%-ного раствора фенолрота в 50%-ном спирте. Среду разливают по 6-7 см 3 в пробирки и стерилизуют 30 мин при 112° С. Среда имеет оранжево-красную окраску. При образовании сероводорода среда окрашивается в черный цвет.
Среда Кларка.
Используется для постановки реакции Фогес-Проскауэра и пробы с метиловым красным для определения окисления глюкозы с образованием 2-кетоглюконата. В 100 см 3 дистиллированной воды растворяют 0,5 г калия гидрофосфата (К 2 НР0 4), 0,7 г пептона, 0,5 г глюкозы. Кипятят 2-3 мин, фильтруют через бумажный фильтр, устанавливают рН 6,9, разливают по пробиркам и стерилизуют 15 мин при
111° С.
Реакцией Фогес-Проскауэра выявляют промежуточный продукт расщепления глюкозы - ацетилметилкарбинол (ацетоин). Для этого испытуемую культуру выращивают на среде Кларка 4-5 дней в 2 пробирках. Одну пробирку культивируют при 25° С, другую при 37° С. Из обеих пробирок по 1 см 3 культуры переносят в другие пробирки и добавляют 0,6 см 3 5%-ного спиртового раствора а-нафтола, смесь перемешивают. Затем добавляют 0,2 см 3 .40%-ного водного раствора КОН. Тщательно перемешивают и инкубируют 1 ч.
Учет реакции проводят через 15 и 60 мин. Положительная реакция - вишневое окрашивание среды.
Тестом с метиловым красным устанавливают снижение рН среды при расщеплении глюкозы до 4,4-6,0. Раствор метилового красного готовят добавлением к 0,1 г метилрота 300 см 3 95%-ного этанола. После растворения красителя добавляют 200 см 3 дистиллированной воды.
Для постановки теста в пробирку с 5 см 3 среды Кларка вносят петлю испытуемой культуры и инкубируют 2-5 сут при 25° С. Затем добавляют 5-6 капель реактива метиловый красный и следят за изменением окраски. При положительном результате (рН 4,0-6,0) среда приобретает красный цвет. При отрицательном результате (рН 6,0-7,0) среда приобретает желтый цвет.
Среда с мочевиной по Кристенсену. Используют для определения способности бактерий к гидролизу мочевины (уреазная активность) с образованием аммиака и углекислоты. В 1000 см 3 дистиллированной воды растворяют 1 г пептона, 5 г натрия хлорида, 2 г калия дигидрофосфата (КН 2 Р0 4), 20 г агара. Смесь стерилизуют 20 мин при 115° С. Затем вносят 1 г глюкозы и 6 см 3 0,2%-ного раствора фенилрота, стерилизуют текучим паром 1 ч, охлаждают до 50° С и асептически добавляют 100 см 3 20%-ного водного раствора мочевины, стерилизованного фильтрацией. Среду разливают по пробиркам и скашивают.
Испытуемую культуру засевают на поверхность скошенного агара и культивируют 1-4 сут. Положительный результат (защелачивание среды) - красно-малиновое окрашивание среды.
Среда Симмонса. Используют для определения способности бактерий утилизировать цитрат как единственный источник углерода. Состав: агар - 20 г, NaCl - 5 г, MgS0 4 х 7Н 2 0 - 0,2 г, К 2 НР0 4 - 1 г, NH 4 х Н 2 Р0 4 - 1 г, C 6 H 5 0 ? Na 3 х 5Н 2 0 - 3 г, бромтимоловый синий - 0,08 г, вода дистиллированная - 1000 см 3 .
В дистиллированной воде растворяют агар. Соли растворяют отдельно в небольшом объеме воды и затем смешивают с агаром, до объема 1000 см 3 . Устанавливают рН 7,2, добавляют 40 см 3 0,2%-ного водного раствора бромтимолового синего. Среду перемешивают, разливают в пробирки по 5-7 см 3 и стерилизуют 15 мин при 121° С. После автоклавирования агар скашивают.
Испытуемую культуру засевают на поверхность агара и инкубируют. При положительном результате отмечают рост культуры на среде и изменение ее цвета с оливкового на синий.
Среда с алгинатом натрия. Используют для определения способности бактерий утилизировать натрия алгинат как единственный источник углерода. Состав среды аналогичен составу среды Симмонса, но вместо натрия цитрата вносится 2,5 г натрия алгината. Положительным считают изменение цвета среды. Микроорганизмы, не обладающие способностью усваивать натрия алгинат, на данной среде не растут.
Среды Гисса. Используют для изучения способности ферментации углеводов с образованием кислоты и газов. Состав: пептон - 10 г, натрия хлорид - 5 г, вода дистиллированная - 1000 см 3 , 0,1%-ный индикатор Андреде, углевод 0,5% (адонит, глицерин, сорбит, дульцит, целлобиоза, раффиноза, трегалоза, салицин, арабиноза, мальтоза, рамноза, ксилоза) или 1,0% (глюкоза, лактоза, маннит, сахароза).
В дистиллированной воде растворяют навески пептона, натрия хлорида, добавляют индикатор, фильтруют через бумажный фильтр, устанавливают рН 7,1-7,2 и стерилизуют 15 мин при 111 ° С. Затем добавляют углевод. Приготовленную среду разливают по пробиркам и стерилизуют
15 мин при 110° С.
Среда для выявления фенилаланиндезаминазы. Состав: сухой дрожжевой экстракт-3 г, натрий хлористый - 5 г, L-фенилалапин - 1 г, Na 2 HP0 4 - 1 г, агар - 12 г, вода дистиллированная - 1000 см 3 . Смешивают воду и дрожжевой экстракт, нагревают, добавляют компоненты и кипятят до расплавления агара, рН среды 7,0-7,2. Горячую среду фильтруют, разливают в пробирки по 2-3 см 3 и стерилизуют 30 мин при 112° С. Среду скашивают.
Испытуемую культуру засевают штрихом по поверхности агара и через сутки инкубации добавляют на поверхность культуры несколько капель 10%-ного водного раствора железа хлорида (FeCl 3). При дезаминировании фенилаланина среда окрашивается в зеленый цвет, при отрицательном результате сохраняется желтое окрашивание.
Среда для выявления β-галактозидазы. В 100 см 3 расплавленного и охлажденного до 40-45° С МПА асептически добавляют 20 см 3 1%-ного водного раствора О-нитрофенил-β-D-галактопиранозид. Среду разливают по пробиркам.
Испытуемую культуру засевают уколом петлей до дна пробирки. Посевы инкубируют 24 ч при 37° С.
При положительной реакции среда окрашивается в желтый цвет одним из конечных продуктов гидролиза О-нитрофенил-β-D-галактопиранозида О-нитрофенолом.
Среды для выявления лизиндекарбоксилазы, орнитиндекарбоксилазы и чргининдегидролазы. Состав: мясная вода - 400 см 3 , пептон - 5 г, глюкоза - 1 г, вода дистиллированная - 600 см 3 , 0,1%-ный спиртовой раствор крезолового красного - 5 см 3 , 1,6%-ный спиртовой раствор бромкрезолового пурпурного - 0,6 см 3 , L-лизин (или орнитин, или аргинин) -10 г.
Мясную воду, пептон, глюкозу и дистиллированную воду смешивают, устанавливают рН 6,0-6,1. Вносят аминокислоту, кипятят 8-10 мин, добавляют индикатор и разливают в агглютинационные пробирки по
3 см 3 . Стерилизуют 30 мин при 110° С. Цвет среды розовый.
Испытуемую культуру засевают в среды с аминокислотами (опыт) и среду безаминокислоты (контроль). Во все пробирки вносят стерильное вазелиновое иасло до получения слоя в 4-5 мм. Пробирки инкубируют 4 дня при 37° С.
При положительной реакции (защелачивание среды) наблюдается синee окрашивание в опытных пробирках и желтое - в контрольной.
Среда для определения пиразинамидазной активности у Y.enterocolitica . Состав: трипсинизированный соевый агар - 30 г, дрожжевой экстракт сухой - 3 г, пиразинкарбоксиамид - 1 г, трисмалат буфер 0,2 М, рН 6,0-1000 см 3 .
Составные части среды смешивают и подогревают на водяной бане до их растворения. Разливают по 5 см 3 в пробирки, стерилизуют 30 мин при 112° С и скашивают.
Среда для определения калъцийзависимости роста у Y. Enterocolitica . В качестве питательной основы используют коммерческую среду для определения чувствительности бактерий к антибиотикам (агар АГВ).
К стерильному расплавленному и охлажденному до 50° С агару добавляют (из расчета на 100 см 3) 8 см 3 0,25 М стерильного натрия щавелевокислого, среду тщательно перемешивают и вносят 4 см 3 0,5 М стерильного раствора магния хлорида. Готовую среду разливают по чашкам Петри.
Определение индолообразования.
Испытуемую культуру выращивают в пробирке с бульоном Хоттингера. В пробирку с культурой вносят 2-3 капли эфира, тщательно ее встряхивают, оставляют в покое до отстаивания на поверхности среды слоя эфира. Осторожно добавляют
0,5 см 3 реактива Эрлиха, выдерживают 5 мин и учитывают результат. При наличии индолообразования слой эфира приобретает розово-красный цвет.
Для приготовления реактива Эрлиха в 95 см 3 96%-ного этанола растворяют 1 г парадиметиламинобензальдегида и добавляют 20 см 3 концентрированной хлористоводородной кислоты (НС1).
Классификация питательных сред производится по их составу и назначению
1.По составу питательные среды делятся на простые и сложные
Различают группу сред общего назначения - простых. К этой группе относят мясо-пептонный бульон (простой питательный бульон), мясо-пептонный агар {простой питательный агар), питательный желатин. Эти среды применяются для выращивания многих патогенных микробов. Среды общего назначения, или простые питательные среды, готовятся обычно из гидролизатов с добавлением пептона и хлористого натрия. Их используют также как основу для приготовления сложных сред.
Также по составу выделяют белковые, безбелковые и минеральные среды. 2. По происхождению среды разделяют на искусственные и естественные (природные ).
Естественные питательные среды могут содержать компоненты животного (например, кровь, сыворотка, жёлчь) или растительного (например, кусочки овощей и фруктов) происхождения.
3.По назначению выделяют консервирующие среды (для первичного посева и транспортировки), среды обогащения (для накопления определённой группы бактерий), среды для культивирования {универсальные простые, сложные специальные и для токсинообразования), среды для выделения и накопления (консервирующие, обогащения и элективные) и среды для идентификации (дифференциальные и элективно-дифференциальные).
Консервирующие питательные среды предупреждают отмирание патогенов и подавляют рост сапрофитов. Наибольшее применение нашли глицериновая смесь, гипертонический раствор, глицериновый консервант с LiCl 2 , раствор цитрата натрия и дезоксихолата натрия.
Среды обогащения для бактерий
Среды обогащения (например, среда Китта-Тароцци, селенитовый бульон, тиогликолевая среда) применяют для накопления определённой группы бактерий за счёт создания условий, оптимальных для одних видов и неблагоприятных для других. Наиболее часто в качестве подобных агентов используют различные красители и химические вещества - соли жёлчных кислот, тетратионат Na+, теллурит К, антибиотики, фуксин, генциановый фиолетовый, бриллиантовый зелёный и др.
Также по назначению различают среды элективные, специальные и дифференциально-диагностические.
Среды элективные (селективные, избирательные, накопления, обогащения). Принцип создания элективных питательных сред основан на удовлетворении основных биохимических и энергетических потребностей того вида микроба, для культивирования которого они предназначены, или на добавление ингибиторов, подавляющих рост сопутствующей микрофлоры. Определенный состав и концентрация питательных веществ, микроэлементов, ростовых факторов при строго определённом значении pH или добавлении ингибиторов обеспечивают оптимальные условия для выращивания одного или нескольких видов микроорганизмов. При посеве на них материала, содержащего смесь различных микробов, раньше всего будет проявляться рост того вида, для которого среда будет элективной. Примером элективных сред являются желчный бульон, селенитовый бульон, среда Плоскирева – для выращивания микробов семейства кишечных, щелочная пептонная вода – для холерного вибриона.
Желчный бульон . К МПБ добавляют 10-20% бычьей желчи. Желчь подавляет рост коков и воздушной флоры, но благоприятна для размножения сальмонелл.
Селенитовый бульон . Состоит из фосфатного бульона с добавлением натриевой соли селенита, которая является ингибитором роста кокковой флоры, кишечной палочки, но не задерживает роста сальмонелл.
Среда Плоскирева . Плотная среда, содержащая ингибиторы кишечной палочки, коков, но благоприятная для роста шигелл и сальмонелл, размножение которых не тормозится бриллиантовым зелёным и желчными солями.
Пептонная вода . Содержит 1% пептона и 0,5% хлористого натрия. Среда является элективной для холерных вибрионов, т.к. они лучше других бактерий размножаются на “голодных средах”, особенно при щелочной реакции, потому что сами выделяют кислые продукты жизнедеятельности.
Специальные среды. Необходимы для культивирования бактерий, не растущих на простых питательных средах. Для некоторых организмов к простым питательным средам необходимо добавлять углеводы, кровь и др. дополнительные питательные вещества. Примерами простых питательных сред являются сахарный бульон и сахарный агар для стрептококка (готовится соответственно из МПБ и МПА, к которым добавляется 0,5-2% глюкозы).
Для пневмококков и менингококков специальной средой являются сывороточный бульон и сывороточный агар (для приготовления сывороточного бульона смешивают 1 часть МПБ с 2 частями свежей сыворотки, для получения, сывороточного агара к расплавленному МПА добавляется 10-25% стерильной лошадиной или бычьей сыворотки).
Дифференциально-диагностические среды используют для определения видовой принадлежности исследуемого микроба, основываясь на особенностях его обмена веществ. По своему назначению дифференциально-диагностические среды разделяют следующим образом:
1. Среды для выявления протеолитической способности микробов, содержащие в своем составе молоко, желатин, кровь и т.д.
2. Среды с углеводами и многоатомными спиртами для
обнаружения различных сахаролитических ферментов.
В состав дифференциально-диагностических сред, предназначенных для выявления сахаролитических свойств и окислительно-восстановительных ферментов, вводят индикаторы: нейтральную красную, кислый фуксин, бромтимоловый синий, водный голубой с розоловой кислотой (ВР). Изменяя свою окраску при различных значениях рН, индикатор указывает на наличие фермента и расщепление введённого в среду ингредиента.
Примеры дифференциально-диагностических сред:
Среда Эндо . Состоит из МПА с добавлением 1% лактозы и обесцвеченного сульфитом натрия основного фуксина (индикатор). Среда Эндо имеет слаборозовый цвет. Используется в диагностике кишечных инфекций для дифференциации бактерий, разлагающих лактозу с образованием кислых продуктов, от бактерий, не обладающих этой способностью. Колонии лактозопозитивных микробов (кишечная палочка) имеют красный цвет вследствие восстановления фуксина. Колонии лактозонегативных микроорганизмов - сальмонелл, шигелл и др. -бесцветны.
К дифференциально-диагностическим средам относятся короткий и развёрнутый пёстрый ряд . Он состоит из сред с углеводами (среды Гисса), МПБ, молока, мясопептонной желатины.
Среды Гисса готовятся на основе пептонной воды, к которой прибавляются химически чистые моно-, ди- или полисахариды (глюкоза, лактоза, крахмал и др.).
Для обнаружения сдвигов рН в результате образования кислот и разложения углевода в среды прибавляют индикатор. При более глубоком расщеплении углеводов образуются газообразные продукты (СО 2 , СН 4 и др.), которые улавливаются при помощи поплавков - маленьких пробирочек, опущенных в среду кверху дном. Среды с углеводами могут готовиться и плотными – с добавлением 0,5-1% агар-агара. Тогда газообразование улавливается по образованию пузырьков (разрывов) в столбике среды.
На МПБ, входящем в пёстрый ряд, обнаруживают продукты, образующиеся при расщеплении аминокислот и пептонов (индол, сероводород). Сероводород обнаруживается путем помещения в МПБ после засева культуры полоски фильтровальной бумаги, пропитанной раствором уксуснокислого свинца. При расщеплении аминокислот, содержащих серу, выделяется сероводород, бумажка чернеет за счёт образования сернистого свинца. Для определения индола можно использовать сложный индикатор. Индол образуется при расщеплении триптофана, и его можно обнаружить при добавлении к культуре, выращенной на МПБ, этого индикатора. При наличии индола МПБ окрашивается в зеленый или синий цвет.
В практических бактериологических лабораториях широко применяют микро- и экспресс-методы для ориентировочного изучения биохимических свойств микроорганизмов. Для этой цели существует множество тест-систем. Наиболее часто используют систему индикаторных бумаг (СИБ). СИБы представляют из себя диски фильтровальной бумаги, пропитанные растворами сахаров или других субстратов в сочетании с индикаторами. Такие диски опускают в пробирку с выросшей в жидкой питательной среде культурой. По изменению цвета диска с субстратом судят о работе фермента. Микро-тест системы для изучения идентификации энтеробактерий представлены одноразовыми пластиковыми контейнерами со средами, содержащими различные субстраты, с добавлением индикаторов. Посев чистой культуры микроорганизмов в такие тест-системы позволяет быстро выявить способность бактерий утилизировать цитраты, глюкозу, сахарозу, выделять аммиак, индол, разлагать мочевину, лизин, фенилаланин и т.д.
Питательный агар, а также основные дифференциально-диагностические среды выпускаются в настоящее время в виде сухих препаратов, содержащих все необходимые составные части. К таким порошкам нужно добавить только воду и сварить, а затем, после разливки, простерилизовать.
Среда Эндо . К 100 мл нейтрального расплавленного 3%-ного мясопептонного агара прибавляют 1 мл 10%-ного водного раствора кристаллического углекислого натрия, выдерживают в текучепаровом аппарате в течение10 мин при температуре 100° С, охлаждают до 60° и стерильно прибавляют 1 г химически чистой лактозы, растворенной в 5 мл стерильной воды, и смесь фуксина с безводным сульфитом натрия. Смесь готовят следующим образом. Растворяют 0,5 г сульфита натрия в 5 мл стерильной воды и добавляют к 1 мл насыщенного спиртового раствора основного кристаллического фуксина до тех пор, пока жидкость не станет бесцветной или слегка розоватой. Обесцвеченную смесь фуксина с сульфитом добавляют к расплавленному агару, и последний принимает розоватый цвет. После тщательного перемешивания (следят за тем, чтобы не образовывалась пена) среду разливают по чашкам. При остывании среда делается цветной, в толстых слоях имеет розоватый оттенок. На этой среде можно легко отличить кишечную палочку, паратифозных бактерий.
Готовят среду перед посевом. Во избежание покраснения ее защищают от света. Выпускается в виде сухого порошка. Способ приготовления указывается на этикетке.
Среда Гисса . Для изготовления индикатораАндредэ берут 100 мл дистиллированной воды, 0,5 г фуксина кислого и 16 мл 4%-ного водного раствора едкого натра. Выдерживают на водяной бане 10 мин. Хранят в темном месте.
Среду с индикатором Андредэ приготовляют следующим образом. Готовят пептонную воду. Для этого берут 1% пептона и 0,5% поваренной соли на определенный объем дистиллированной воды. Кипятят до растворения пептона, фильтруют через бумажный складчатый фильтр, устанавливают рН 7,0-7,2. После подщелачивания 10%-ным раствором NаОН снова кипятят в течение 10 мин, фильтруют и к готовой 1%-ной пептонной воде (рН 7,0-7,2) добавляют 1% индикатора Андредэ. К среде с индикатором добавляют требуемые углеводы или многоатомные спирты в количестве 0,5% - 1% (лактозу, глюкозу, сахарозу, маннит, дульцит и др.). Среды разливают по пробиркам, снабженным для учета образования газа бродильными трубочками. Вместо трубочек иногда помещают кусочки ваты - 0,02 г на пробирку. Проводят дробную стерилизацию при температуре 100° С в течение 20 мин три дня подряд.
Правильно приготовленная среда имеет соломенно-желтый цвет.
Среда Кесслера . В 1 л водопроводной воды вносят 50 мл свежей бычьей желчи и 10 г пептона. Кипятят на водяной бане 15 мин, постоянно взбалтывая. После полного растворения среду фильтруют через вату и добавляют 10 г лактозы. Доводят рН до 7,7. К 1 л среды добавляют 4 мл 1 %-ного водного раствора генцианвиолета и разливают в пробирки с поплавками. Стерилизуют в автоклаве при избыточном давлении 0,1 МПа в течение 15 мин.
Определение рН питательных сред
Для культивирования микробов на искусственных питательных средах особое значение имеет концентрация водородных ионов, так как каждый вид микроба может развиваться только при определенной кислотности или щелочности. Большинство бактерий приспособлено к росту и размножению в нейтральной или слабощелочной среде (рН 7,0-7,6).
Для определения реакции питательной среды применяют два метода: электрометрический (с помощью рН-метра) и колориметрический. В лабораторной практике чаще всего используется наиболее простой колориметрический метод по Михаэлису, основанный на изменении цвета индикатора вследствие диссоциации его в зависимости от концентрации водородных ионов в среде. При определении рН по Михаэлису применяют индикаторы нитрофенолового ряда. Ввиду того, что для выращивания микробов готовят среды слабощелочной реакции, при определении рН среды в качестве индикатора используют метаннитрофенол, который позволяет определять рН в пределах от 6,8 до 8,4. Растворы индикатора готовят на дистиллированной воде и хранят во флаконах из темного стекла с притертой пробкой.
Контрольные вопросы :
Состав питательных сред.
Как культивируют в лабораторных условиях микроорганизмы?
Какие бывают питательные среды по консистенции?
Как различают питательные среды по происхождению?
Плотные питательные среды и их характеристика.
Сухие питательные среды и их характеристика.
Углеводные питательные среды, их характеристика.
Автоклавирование.
Стерилизация текучим паром.
Пастеризация.
Стерилизация фильтрованием.
Как готовят МПБ, МПЖ, МПА?